Olá, sou o Dr. Daniel Omote. Minha jornada como especialista em retina e genética ocular pela USP me ensinou que, por trás de cada diagnóstico de Degeneração Macular Relacionada à Idade (DMRI), existe uma história de vida que merece ser preservada. Neste artigo, vamos mergulhar profundamente no que há de mais moderno sobre esta condição, desde a biologia celular até os exames para diagnóstico da DMRI que salvam visões diariamente.
Primeiro, por que é importante entender este assunto?
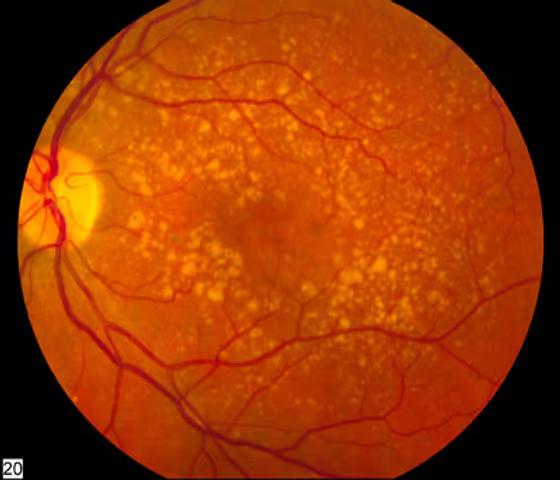
A DMRI causa perda importante da visão central. Muitas vezes, aceitamos as mudanças que vêm com a idade como inevitáveis — os cabelos brancos, as dores nas articulações... Mas quando se trata da nossa visão, o "desgaste" natural do tempo pode ter um nome específico e sério: Degeneração Macular Relacionada à Idade (DMRI). Como especialista em retina pela USP, vejo diariamente a angústia de pacientes que notam o mundo ao seu redor perder a nitidez. Por isso, antes de falarmos sobre tratamentos e exames, preciso que você entenda exatamente o que é essa condição e quais sinais o seu olho envia quando algo não vai bem.